Introducción
Desde el siglo V a.
de C. la humanidad ha escuchado hablar de átomos, como las partículas
fundamentales de la materia.
Sin embargo, debido
a que los átomos son tan pequeños, no es posible verlos a simple vista, por
esta razón, se han propuesto varios modelos y teorías acerca de cómo son estas
partículas fundamentales.
Un modelo atómico es una representación estructural de un átomo, que trata de explicar su comportamiento y propiedades.
La investigación del proceso de electrólisis
posibilitó inferir que la materia es de naturaleza eléctrica.
Los experimentos sobre descargas eléctricas en
gases a baja presión permitieron comprobar que los átomos están formados por
partículas materiales negativas (electrones) y positivas (protones). A partir
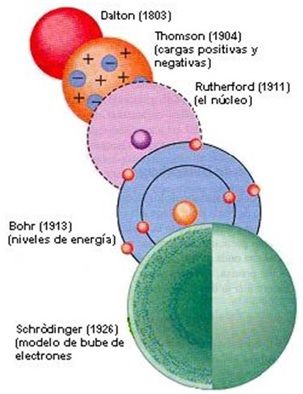
de estos descubrimientos Thomson
propuso el primer modelo atómico.
El descubrimiento de la radiactividad
posibilitó la realización de experiencias que llevaron a Rutherford,
a sostener que el átomo tiene un núcleo central con carga positiva.
El análisis de los espectros atómicos
producidos por el hidrógeno permitió a Bohr proponer una
hipótesis, basada en la teoría cuántica de Planck,
que supone que los electrones están ubicados en órbitas circulares, denominadas
niveles de energía. Asimismo, fue posible definir dos números importantes
(número atómico y número másico), establecer el concepto de isótopos y
profundizar la noción de iones.
En razón de que la hipótesis de Bohr
no explicaba nuevos hechos experimentales, Sommerfeld
sugirió que los electrones también describen órbitas elípticas.
El estudio del espectro de diferentes
elementos llevó a concebir la existencia de subniveles energéticos.
Al sostener De Broglie
que las partículas muy pequeñas como los electrones presentan a dualidad
onda-partícula, Heisenberg
enunció el principio de incertidumbre. A partir de este principio y aplicando
el cálculo de probabilidades se llegó a la noción de orbital atómico en
reemplazo del concepto de órbita. Esta concepción del átomo surge al resolver
la ecuación de onda de Schrödinger
que permitió introducir los números cuánticos.


No hay comentarios.:
Publicar un comentario